Термостойкость кислородных щелочных вольфрамовых и молибденовых бронз
Аннотация
Дата поступления статьи: 20.12.2012Оксидные бронзы МхЭО3 (М – Na,K; Э – W,Mo) представляют неорганические материалы техники и химической технологии. Их свойства, например, стабильность в широком интервале температур, представляют большой практический интерес (электроды топливных элементов, приборы электронной техники и другие).В статье приведены результаты исследования термостойкости натриевых и калиевых вольфрамовых и молибденовых бронз на воздухе и в вакууме при 20–1110°С. Образцы получены электролизом расплавов изополивольфраматов и – молибдатов натрия, калия. Данные для бронз Na0.92WO3 , Na0.68WO3 , Na0.53WO3 , Na0.15MoO3 , K0.3MoO3 получены методами термогравиметрического-дифференциально-термического анализа (TG-DТА). Установлены области стабильности у Na0.92WO3 : 20–700°С, у МхМоО3 : 300–500°С. Сделан вывод о корреляции нестехиометрии химического состава бронз и оксидов ЭОх, играющих важную роль в формировании структуры бронз переходных металлов.
Ключевые слова: оксидные щелочные бронзы, вольфрам, молибден, термостойкость, нестехиометрия, термический анализ
Щелочные оксидные бронзы вольфрама, молибдена, других переходных металлов весьма важны как неорганические материалы современной техники и объекты изучения и применения наноразмерных структур [1-4]. В этой связи необходимо рассмотреть некоторые их свойства, представляющие большой интерес. Использование щелочных вольфрамовых и молибденовых бронз в качестве электродов топливных элементов и в электронной технике требует знания их термостойкости на воздухе и в вакууме. Нами проведено испытание на воздухе для некоторых образцов бронз Na0.92WO3, Na0.53WO3, K0.3MoO3, Na0.9Mo6O17 (рис. 1-3). Первая при нагревании от 20 до 870°С обнаруживает одно эндотермическое превращение при 725°С, соответствующее фазовому переходу WO3. Кривая ДТГ фиксирует потерю веса, отвечающую выделению адсорбированных влаги и газов (рис. 1). У бронзы Na0.53WO3 кривая потери веса при 500°С испытывает резкий подъем вследствие окислительного процесса. Эндоптики при 742 и 840°С принадлежат WO3 и W18O49, экзоэффект при 1120°С обусловлен полным окислением образца до Na2WO4 и WO3. Соответствие бронзы Na0.53WO3 и нестехиометрического оксида W18O49 подтверждает практическая идентичность в них зарядовых чисел вольфрама n = +5,47 и + 5,44.
Многосторонние исследования оксидов вольфрама, молибдена и других переходных элементов показали, что их следует отнести к соединениям с малой нестехиометрией и статистическим расположением дефектов. Основой структур таких оксидов, общей с WO3 и MoO3, являются октаэдры ЭО6, реже тетраэдры ЭО4 и
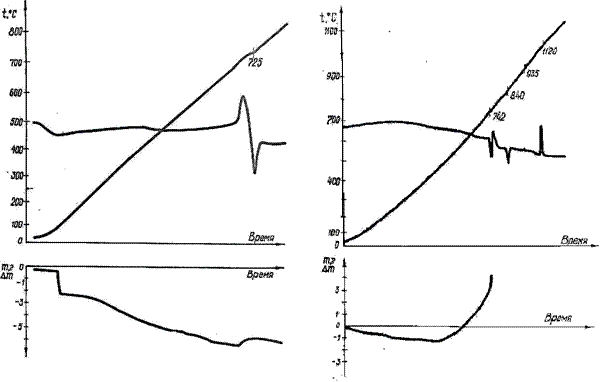
Рис.1 Термограмма и дериватограмма Рис.2 Термограмма и дериватограмма
вольфрамовой бронзы Na0,92WO3 вольфрамовой бронзы Na0,53WO3
1 2
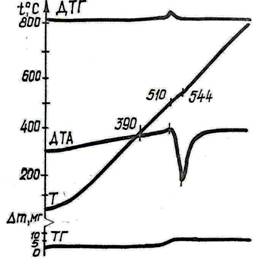
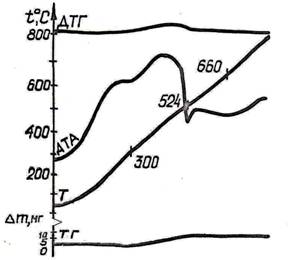
Рис.3. Термограммы и дериватограммы молибденовых бронз:
1 - К0,3МоО3 ; 2 - Na0,9Mo6O17
пентагональные бипирамиды [5]. Химический состав оксидов («фаз Магнели») приведен в таблице, наряду с составами исследованных бронз. Сопоставив значения зарядов n+ в формулах бронз и оксидов, наблюдаем их явное сходство, например, Na0.53WO3 с W18O49, Na0.37WO3 со средней величиной 0.5n+ (W18O49 + W20O58) = 5,62 и др. То же и у соединений молибдена: K0.3MoO3 и Mo8O23; Na0.15MoO3 и Mo9O26 (табл.). Подобные оксиды играют существенную роль в формировании сложного химического состава бронз при их получении методами восстановления.
Термостойкость в атмосферных условиях апробирована у синей бронзы K0.3MoO3 и Na0.9Mo6O17 (красной). Анализ кривых ДТА и ДТГ (рис. 3) показал, что при 400–510°С у калиевой и 300–500°С у натриевой бронз наблюдается увеличение массы образцов вследствие взаимодействия с О2 атмосферы и перехода в щелочные изополимолибдаты и MoO3, например, по реакциям:
20К0.3МоО3+1,5О2 = 3К2Мо4О13 + 8МоО3,
20Na0.9Mo6O17 + 14,5O2 = 9Na2Mo4O13 + 84MoO3
Таблица
Состав нестехиометрических оксидов и щелочных оксидных бронз вольфрама, молибдена
|
Соединение |
Wn+ |
Соединение |
Mon+ |
|
Na0.92WO3 |
5,08 |
Na0.92Mo6O17 |
5,85 |
|
Na0.53WO3 |
5,47 |
||
|
Na0.68WO3 |
5,32 |
K0.3MoO3 |
5,70 |
|
Na0.37WO3 |
5,63 |
Mo4O11 |
5,50 |
|
W18O49 |
5,44 |
Mo5O14 |
5,60 |
|
W20O58 |
5,80 |
Mo8O23 |
5,75 |
|
W40O118 |
5,90 |
Mo9O26 |
5,78 |
|
WO2 |
4,00 |
MoO2 |
4,00 |
Подтверждением этого является совпадение эндопиков кривых ДТА (544, 524°С) обеих бронз с температурами двойных эвтектик систем K2MoO4 – MoO3 и Na2MoO4 – MoO3 с высоким содержанием MoO3, а также наличие в спектре РФА продукта окисления бронзы K0.3MoO3 набора дифракционных линий К2Мо4О13 и МоО3.
В вакууме исследовано нагревание бронз Na0.68WO3 и Na0.37WO3 (рис. 4, 5). Установлено, что температуры плавления образцов – 1072 и 1138°С соответственно. Различие точек плавления связано с увеличением содержания вольфрама в синей бронзе. Эндоэффекты при 500°, 536°, 590°С, вероятно, связаны с разложением бронз до Na2WO4, WO3, WO2 и других продуктов распада.
Нестехиометрия оксидов WOx с 2,66<х<3,0, близких по природе к щелочным вольфрамовым бронзам, влияет на их электро- и фотохромные свойства, представляющие собой окислительно-восстановительные процессы [6]. Электро– и фотохромный эффекты – обратимые изменения цвета материала под действием электричесокого тока или излучения. Данные процессы стали частью научно-технического направления – ионики твердого тела и интенсивно исследуются в наше время.
Автор работы [6] Тутов указывает, что оксиды WO3-x являются полупроводниками n-типа проводимости. Стойкость фаз WO3-x (таблица) подтверждается в работах многих авторов, изучавших структуру, свойства, применение в технике и нанотехнологии [7, 8]. В [7] Салье приводит кристаллическую структуру и парамагнитные свойства трех низкотемпературных фаз WO3-x – γ, δ, ε низших сингоний для 240–250°К (δ-фаза) и
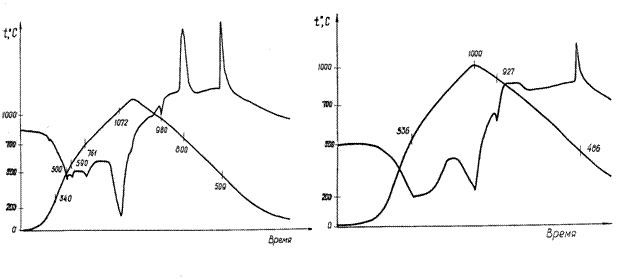
Рис.4. Термограмма бронзы Na0,68WO3 Рис. 5. Термограмма бронзы Na0,37WO3
(вакуум) (вакуум)
5К (ε-фаза). В [8] Бурачас с соавт. нашли, что в регулярной решетке PbWO4 присутствуют кластерные дефекты оксидов WO3-x, влияющие на окраску кристаллов, что важно учитывать при получении оптически прозрачных кристаллов – детекторов γ-радиационной стойкости блоков.
Большое значение в развитие химии оксидов вольфрама вносят исследования их в виде наноструктур – нитей, трубок, стержней, пленок, сеток [9–12]. Получено подтверждение существования фаз W18O49, W3O8, WO, WO2, WO3 в виде наносоединений, найдены области их использования в современной технике.
На основании представленных данных можно сделать вывод о корреляции зарядов Wn+ в интервале +(5,3 – 5,9) у бронз NaxWO3 и оксидов WO3-x, что объясняет роль этих оксидов в нестехиометрическом характере кислородных щелочных бронз.
Литература:
- Оксидные бронзы (Под ред. ак. В.И. Спицына) [Текст]. М., Наука, 1982, С. 40–75, 183–188.
- Kakali G., Ramanujachary K.V., Greenblatt M. Application of alkali metal molybdenum bronzes as Na+-ion selective sensors up to 70°C // Sensors and Actuators B, 2001. – V. 79. – P. 58–62.
- Волков В.Л., Захарова Г.С., Кузнецов М.В. Наностержни MoO3-δ [Текст] // Журн. неорган. хим. 2008. – Т. 53. – №11. – С. 1807–1811.
- Малышев В.В. Механизмы электровосстановления и электроосаждение покрытий металлов VI–А группы из ионных расплавов [Текст] // Физикохимия поверхности и защита материалов. 2009. Т. 45. №4. С. 339–357.
- Bursill L.A. Structure of small defects in nonstoichiometric WO3-x // J. Sol. State Chem. 1983. – V. 48. – P. 256–271.
- Кукуев В.И., Тутов Е.А., Солодуха А.М. и др. Получение электрохромных пленок на основе триоксида вольфрама методом испарения и конденсации в вакууме [Текст] // Электронная техника. Сер. 6: Материалы. 1985. – Вып. 6, – С. 3–6.
- Salje E.K.H., Rehmann S., Pobell F. et al. Ctystal structure and paramagnetic behaviour of ε-WO3-x // J. Phys. Condens. Matter., 1997. – V. 9. – P. 6563 – 6577.
- Бурачас С.Ф., Васильев А.А., Ипполитов М.С. и др. Физическая природа температурной зависимости радиационной стойкости блоков детектирования на основе кристаллов вольфрамата свинца // Труды междунар. конф. Инженерия сцинтилляционных материалов и радиационные технологии. ISMART – 2008. Харьков. Украина. 17–21.11.2008 г., C.1–23. – Режим доступа: http: //www.2008.ismart.kharkov.ua >presentations /20/ (доступ свободный) – Загл. с экрана. – Яз. рус.
- Soultanidis N., Barron A.R. TGA/DSC – FTIR characterisation of oxide nanoparticles. May 23, 2009. P. 1–9. – Режим доступа: // http: //cnx.org/content/m23038/1.2/ (доступ свободный) – Загл. с экрана. – Яз. англ.
- Govender M., Shikwambana L., Mwakikunga B.W. et al. Formation of tungsten oxide nanostructures by laser pyrolysis: stars, fibres and spheres // Nanoscale Research Letters, 2011. – V. 6: 166. – P. 1–8.
- Deng X., Quek S.Y., Biener M.M. et al. Selective thermal reduction of single-layer MoO3 nanostructures on Au (111) // Surface Science, 2008. – V. 602. – P. 1166–1174.